FDA食品接觸測(cè)試是什么
- 時(shí)間:2021-10-29作者:上海沙格醫(yī)療科技有限公司武漢分公司瀏覽:346
上海沙格醫(yī)療科技有限公司武漢分公司專注于IVDR,CE認(rèn)證,MDR,QSR820驗(yàn)廠,英國(guó)UKCA認(rèn)證等
詞條
詞條說(shuō)明
QSR 820質(zhì)量體系規(guī)范中描述了現(xiàn)行的生產(chǎn)管理規(guī)范的要求(CGMP)。本規(guī)范要求規(guī)定了所有醫(yī)用器械成品在設(shè)計(jì)、制造、包裝、標(biāo)簽、貯存、安裝和服務(wù)中使用的方法,設(shè)施和控制。這些要求是為了確保醫(yī)療器械成品的*和有效,并遵從美國(guó)食品藥品和化妝品法。本規(guī)范提出了適用于醫(yī)療器械成品制造商的基本要求,如果某制造商只進(jìn)行本規(guī)范規(guī)定的一部分操作,而不進(jìn)行其他操作,則該制造商僅需執(zhí)行適用于他所進(jìn)行操作的那些要求
ISO13485認(rèn)證是全世界醫(yī)療設(shè)備制造商(如:美國(guó)、日本、加拿大、歐盟)較為接受的標(biāo)準(zhǔn)。這一標(biāo)準(zhǔn)包括專門針對(duì)這一行業(yè)的要求,并為諸如醫(yī)療設(shè)備、主動(dòng)型醫(yī)療設(shè)備、主動(dòng)型移植設(shè)備和無(wú)菌醫(yī)療設(shè)備等其他的術(shù)語(yǔ)做了定義。ISO13485認(rèn)證支持那些生產(chǎn)制造或使用醫(yī)療產(chǎn)品和服務(wù)的企業(yè),幫助這些企業(yè)減少不可預(yù)期的風(fēng)險(xiǎn)。該體系力圖提高企業(yè)在顧客及*組織眼中的聲譽(yù)。ISO134852003已正式頒布,該標(biāo)準(zhǔn)將取消
收到FDA驗(yàn)廠通知,需要做哪些準(zhǔn)備工作?
FDA驗(yàn)廠即工廠檢查,F(xiàn)DA屬下的CDRH(器材與放射性健康中心)是職業(yè)承擔(dān)醫(yī)療設(shè)備企業(yè)管理方法的**部門,其依據(jù)FDA的受權(quán),分配檢查員到各企業(yè)開(kāi)展工廠檢查。驗(yàn)廠抽樣檢查標(biāo)準(zhǔn) --依據(jù)法律法規(guī),對(duì)未免除QSR 820的設(shè)備的生產(chǎn)制造企業(yè),開(kāi)展常規(guī)檢查;(大部分狀況) --II類器材或者有510(K)申請(qǐng)注冊(cè)的用具的企業(yè),非常*被抽中; --為海外大企業(yè)做OEM的企業(yè); --商品在美國(guó)銷售市場(chǎng)產(chǎn)
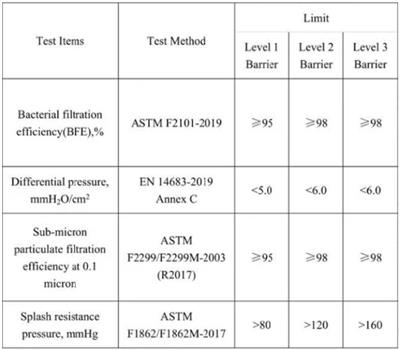
很多人對(duì)于fda不是很了解,fda是美國(guó)食品藥品監(jiān)督管理局,美國(guó)本國(guó)生產(chǎn)以及進(jìn)出口的相關(guān)產(chǎn)品,都要受到fda的監(jiān)管,這也是在辦理fda的時(shí)候所要掌握好的,在進(jìn)行fda辦理時(shí),fda的標(biāo)準(zhǔn)需要了解清楚,那么fda標(biāo)準(zhǔn)指的是什么?如何測(cè)試?產(chǎn)品進(jìn)行fda的認(rèn)證,主要是根據(jù)fda的標(biāo)準(zhǔn)來(lái)進(jìn)行的,根據(jù)fda的相關(guān)規(guī)定,進(jìn)行fda的注冊(cè)和檢測(cè),食品、藥品、化妝品等在進(jìn)行fda辦理的時(shí)候需要進(jìn)行fda的注冊(cè),
聯(lián)系方式 聯(lián)系我時(shí),請(qǐng)告知來(lái)自八方資源網(wǎng)!
聯(lián)系人: 蔣小姐
電 話: 17717017570
手 機(jī): 18007141921
微 信: 18007141921
地 址: 湖北武漢江漢區(qū)新華西路武漢菱角湖萬(wàn)達(dá)廣場(chǎng)A區(qū)A.幢A3單元12層5號(hào)
郵 編:
網(wǎng) 址: viacertt.cn.b2b168.com
相關(guān)推薦
相關(guān)閱讀
1、本信息由八方資源網(wǎng)用戶發(fā)布,八方資源網(wǎng)不介入任何交易過(guò)程,請(qǐng)自行甄別其真實(shí)性及合法性;
2、跟進(jìn)信息之前,請(qǐng)仔細(xì)核驗(yàn)對(duì)方資質(zhì),所有預(yù)付定金或付款至個(gè)人賬戶的行為,均存在詐騙風(fēng)險(xiǎn),請(qǐng)?zhí)岣呔瑁?
- 聯(lián)系方式
聯(lián)系人: 蔣小姐
手 機(jī): 18007141921
電 話: 17717017570
地 址: 湖北武漢江漢區(qū)新華西路武漢菱角湖萬(wàn)達(dá)廣場(chǎng)A區(qū)A.幢A3單元12層5號(hào)
郵 編:
網(wǎng) 址: viacertt.cn.b2b168.com
- 相關(guān)企業(yè)
- 北京同基偉業(yè)管理咨詢有限公司
- 合肥傲宇認(rèn)證有限公司
- 鎮(zhèn)江九州管理咨詢有限公司
- 中包測(cè)試技術(shù)(廣東)有限公司
- 上海序亭通信科技有限公司
- 廣東啟智企業(yè)服務(wù)有限公司
- 浙江三洲檢測(cè)認(rèn)證有限公司
- 深圳市中檢聯(lián)標(biāo)技術(shù)服務(wù)有限公司
- 蘇州天標(biāo)檢測(cè)技術(shù)有限公司
- 臺(tái)州鑫程認(rèn)證有限公司
- 商家產(chǎn)品系列
- 筆記本回收
- 服裝道具
- 服裝設(shè)計(jì)
- 復(fù)印機(jī)維修
- 復(fù)印機(jī)租賃
- 工商年檢
- 公關(guān)策劃
- 公關(guān)服務(wù)
- 公司注冊(cè)
- 管理培訓(xùn)
- 管理咨詢
- 廣告策劃
- 廣告代理
- 廣告發(fā)布
- 廣告設(shè)計(jì)
- 國(guó)內(nèi)貨運(yùn)運(yùn)輸
- 國(guó)內(nèi)勞務(wù)派遣
- 沙盤模型設(shè)計(jì)制作
- 商標(biāo)注冊(cè)
- 商標(biāo)轉(zhuǎn)讓
- 商務(wù)翻譯
- 商務(wù)服務(wù)
- 商務(wù)租車
- 設(shè)備租賃維修
- 手板模型
- 形象策劃
- 虛擬主機(jī)
- 移民咨詢
- 印刷機(jī)維修
- 秘書(shū)服務(wù)
- 產(chǎn)品推薦
- 資訊推薦